Lunes, 27 de Abril del 2020
El propósito de hoy es explicar que los compuestos orgánicos más simples son los hidrocarburos, los cuales forman 3 grupos con características propias.
SESIÓN 4
HIDROCARBUROS CON ENLACE SIMPLE
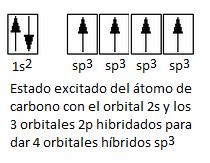
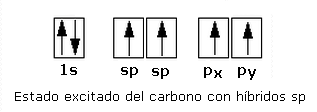
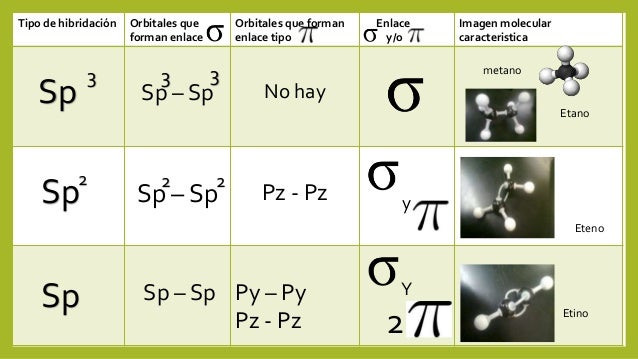
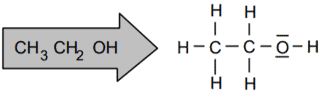
Observa las siguientes imágenes:



Después de observar las imágenes se les plantea las siguientes preguntas: (en la classroom)
- ¿Qué es lo que se observa?
- ¿Qué se extrae?
- ¿Cómo se habrá formado?
- ¿Para qué se utiliza?
- ¿Cómo se relaciona con los hidrocarburos?
- ¿Qué problemas puede causar su extracción?
A continuación se te invita a que realices la observación del vídeo "Los Hidrocarburos" https://www.youtube.com/watch?v=l73LOeNwke8
Después de observar el vídeo responde a las siguientes preguntas: (en la classroom)
- ¿Qué son los hidrocarburos?
- ¿De qué están hechos?
- ¿Cómo se presentan en la naturaleza?
- ¿Por qué se dice que son orgánicos?
- ¿Dónde se encuentran?
A continuación revisa y lee la siguiente información sobre los hidrocarburos a partir de ella registra las ideas más importantes en tu cuaderno de trabajo.
Posteriormente, a partir de la ideas registradas elabora un organizador visual considerando la nomenclatura, formulación, propiedades y ejemplos de alcanos. (en la classroom)
Luego se te presenta una lectura referente al "Gas Propano" subraya o resalta los aspectos que consideres más importantes y responde a las preguntas planteadas: (en la classroom)
Completando la información te invito a que observes el siguiente vídeo tutorial que reforzará la formulación y nomenclatura de los alcanos
Finalmente resuelve la ficha de aplicación 3 sobre formulación y nomenclatura de los hidrocarburos saturados o alcanos. (en la classroom)
Luego se te presenta una lectura referente al "Gas Propano" subraya o resalta los aspectos que consideres más importantes y responde a las preguntas planteadas: (en la classroom)
- ¿Qué tipo de hidrocarburo es y por qué?
- ¿En qué se usa?
- ¿Dónde se encuentra?
- ¿Cuál es su procedencia? o ¿Cómo se formó?
- ¿Qué características presenta que lo hacen tan útil?
Completando la información te invito a que observes el siguiente vídeo tutorial que reforzará la formulación y nomenclatura de los alcanos
Fecha de entrega: hasta el Domingo, 03 de Mayo del 2020.
·
·